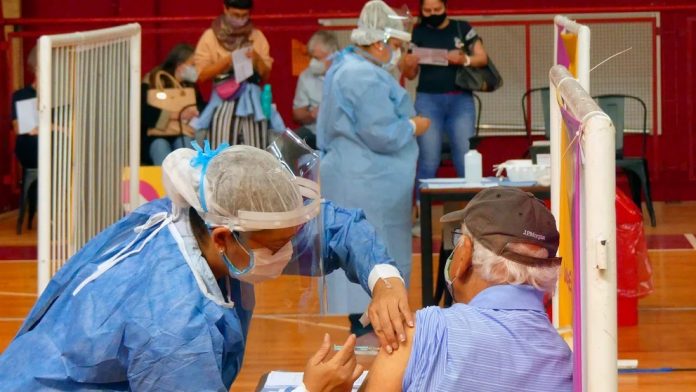
El 56% de la humanidad ya recibió la primera dosis de la vacuna contra el COVID-19. El 45% tiene hoy el esquema completo con la inmunización. Un 3,2% aceptó recibir una tercera dosis después de un tiempo de haber completado el esquema y para aumentar aun más la protección contra el coronavirus y reducir el riesgo de hospitalización y muerte.
Un estudio realizado en el Reino Unido y publicado en la revista especializada The Lancet demostró que seis vacunas diferentes contra el Covid-19 son seguras y eficaces cuando se utilizan como dosis de refuerzo. Es decir, recibir una vacuna diferente como tercera dosis funciona bien.
En el estudio de comparación de las siete marcas de vacunas diferentes, los investigadores británicos descubrieron que la mayoría provocaban una fuerte respuesta inmunitaria cuando se aplicaban como terceras dosis. Entre ellas, las inyecciones de vacuna de ARN mensajero de Moderna y Pfizer-BioNTech fueron las que provocaban las mayores respuestas.
Se trató de un ensayo en Fase II que analizó la seguridad y eficacia de siete vacunas administradas después de dos dosis iniciales de la vacuna de Oxford-AstraZeneca o de Pfizer-BioNTech. Las vacunas incluidas en el estudio fueron las producidas por Oxford-AstraZeneca, Pfizer-BioNTech, Novavax, Johnson & Johnson, Moderna, Valneva y Curevac.
Los funcionarios de los Centros para el Control y la Prevención de Enfermedades, preocupados por los informes preliminares sobre Ómicron, dijeron el lunes que todos los adultos deberían recibir la dosis de refuerzo. El primer caso confirmado de infección con esa variante fue registrado el miércoles en San Francisco, en una persona que regresó de un viaje a Sudáfrica el 22 de noviembre. La persona, quien presentó síntomas leves y se dijo que estaba mejorando, tenía el esquema completo de vacunación, pero no había recibido una dosis de refuerzo.
En el estudio participaron 2.878 adultos mayores de 30 años, y concluyó que ninguna de las siete vacunas tuvo problemas de seguridad cuando se la usó como dosis de refuerzo. La fatiga, los dolores de cabeza y el dolor en el lugar de la inyección fueron los efectos secundarios más comunes, y se registraron sobre todo en personas jóvenes. Un total de 912 participantes experimentaron efectos adversos a causa de la vacuna de refuerzo, de los cuales 24 fueron graves durante el estudio.
El profesor Saul Faust, líder del ensayo y director del Centro de Investigación Clínica NIHR del Hospital Universitario Southampton, en el Reino Unido, dijo: “Nuestros datos sobre los efectos secundarios muestran que las siete vacunas son seguras para su uso como tercera dosis, con niveles aceptables de reactogenicidad, es decir, efectos secundarios inflamatorios como dolor en el lugar de la inyección, dolor muscular y fatiga”.
Además, agregó: “Las siete aumentaron significativamente los niveles de anticuerpos contra la proteína de la Espiga después de dos dosis de AstraZeneca. Sin embargo, sólo seis lo hicieron también tras dos dosis de Pfizer-BioNTech (AstraZeneca, Pfizer-BioNTech, Moderna, Novavax, Janssen y CureVac). También hubo grandes variaciones en la respuesta con diferentes refuerzos”.
Tras el análisis de los resultados, el doctor Faust comentó también: “Es realmente alentador que una amplia gama de vacunas, que utilizan diferentes tecnologías, muestren beneficios como dosis de refuerzo de cualquiera de estas vacunas. Esto da confianza y flexibilidad en el desarrollo de programas de refuerzo aquí y en todo el mundo, con otros factores como la cadena de suministro y la logística también en juego”.
Los participantes gozaban de “buena salud”, según los autores del estudio, y fueron reclutados en 18 localidades diferentes del Reino Unido. Alrededor de la mitad había recibido dos dosis de la vacuna de Oxford-AstraZeneca, mientras que la cohorte restante había sido vacunada con la vacuna de Pfizer-BioNTech. Alrededor de la mitad de los participantes en el estudio eran mayores de 70 años. Algunos individuos fueron incluidos en un grupo de control y se les administró una vacuna antimeningocócica como placebo.
Infobae